Você está com dificuldades para interpretar Gráficos de Cinética Química? 📉
Dominar os exercícios que envolvem a Teoria das Colisões e a análise gráfica é um passo fundamental para quem deseja gabaritar as provas de Ciências da Natureza no ENEM e nos principais vestibulares. 🚀
Nesta lista exclusiva elaborada pelo Olhar Químico, foram selecionados exercícios que vão muito além do básico, focando exatamente no que você precisa dominar!
Aqui, você encontrará:
💥 O papel crucial da Energia de Ativação e do Complexo Ativado;
📊 A interpretação correta de Diagramas de Energia (Endotérmicos e Exotérmicos);
⚡ Os impactos reais do Catalisador na velocidade da reação.
Tudo isso acompanhado de gabarito com resolução detalhada!
Prepare o seu material e vamos transformar a Cinética Química e esses gráficos em nota máxima! ✍️
QUESTÃO 1
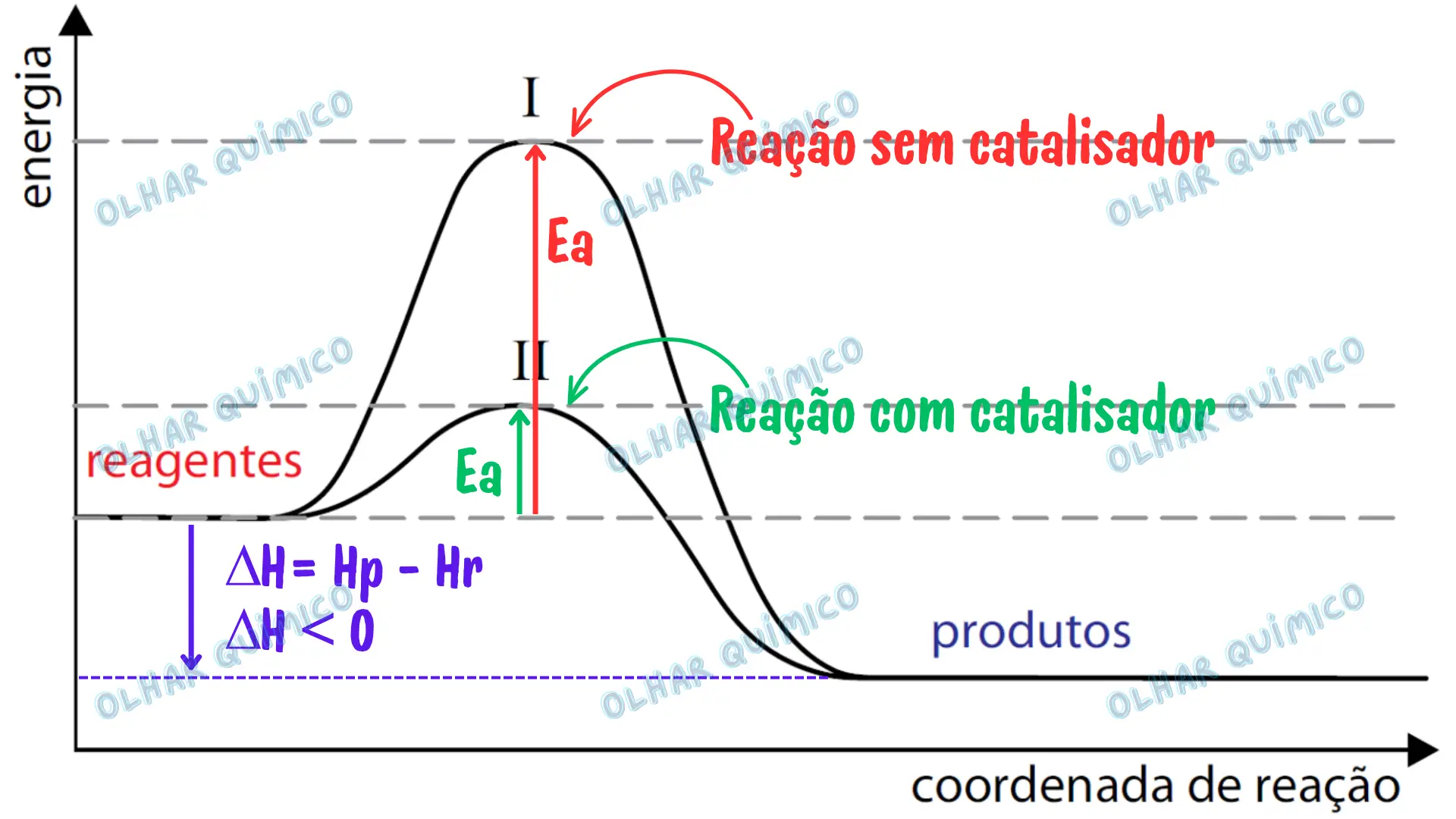
(FAMERP – SP) O estudo cinético de determinado processo químico permitiu a construção de coordenadas de reação como a ilustrada no gráfico.
De acordo com a análise do gráfico, verifica-se que:
(A) a reação ocorre pelo caminho II devido à presença de um catalisador liberando energia, diferentemente do caminho I, que é endotérmico.
(B) quando a reação ocorre pelo caminho I, o reagente A2 é consumido mais rapidamente do que quando ocorre pelo caminho II.
(C) a reação é endotérmica, sendo absorvida a energia dada por (x – z) por mol de A2 consumido.
(D) devido à atuação do catalisador, o caminho II apresenta menor energia de ativação, igual a y, do que o caminho I, cuja energia de ativação é dada por x.
(E) a reação é exotérmica e libera energia dada por (x + z) por mol de A2 consumido.
QUESTÃO 2
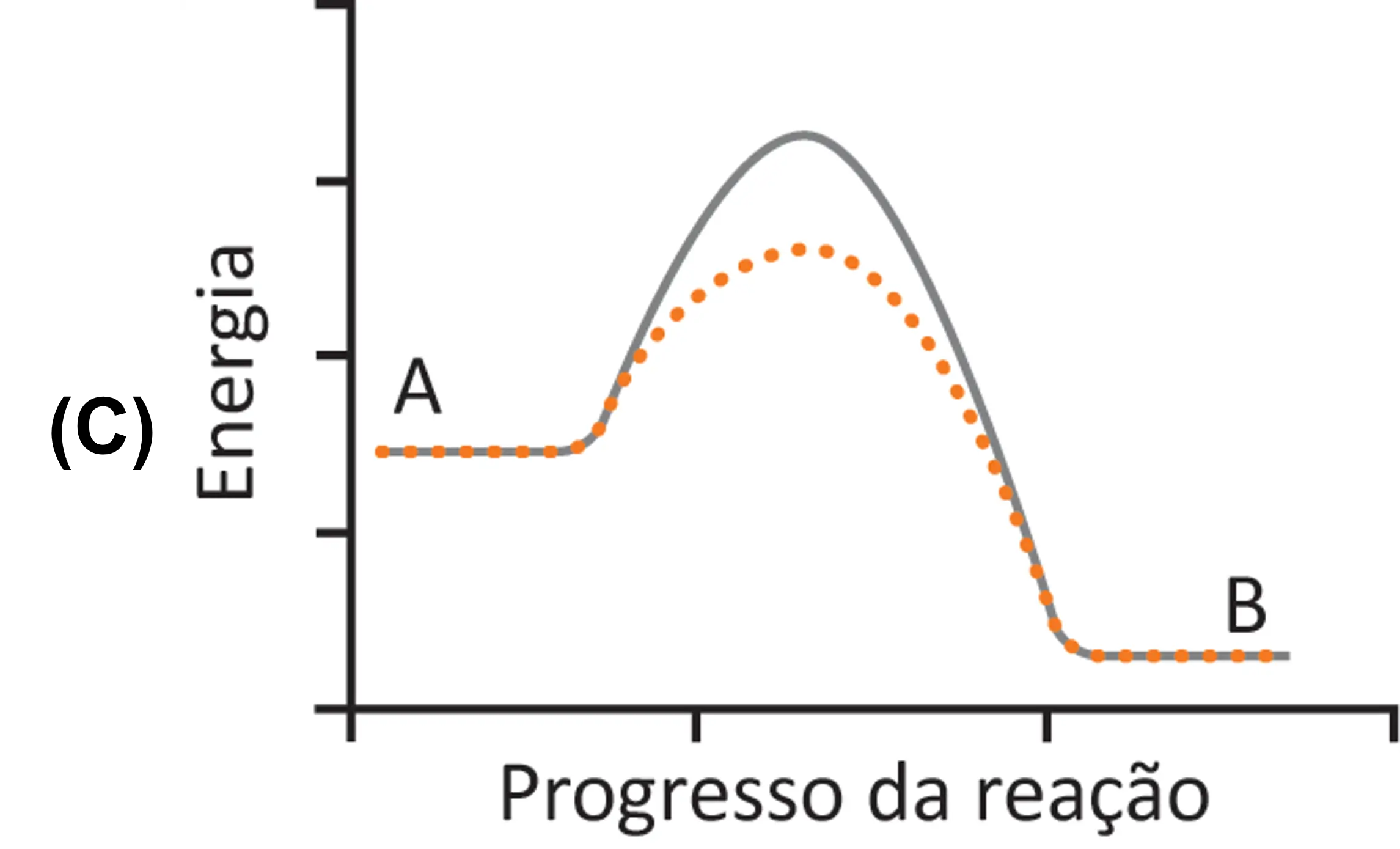
(UFRGS – RS) Uma professora, ao introduzir o conceito de energia de ativação, projetou em sua aula o seguinte modelo teórico.
Adaptado de: MARTORANO, S. A. A. A transição progressiva dos modelos de ensino sobre cinética química a partir do desenvolvimento histórico do tema. 2012. Tese (Doutorado em Ensino de Química) Ensino de Ciências (Física, Química e Biologia), Universidade de São Paulo, São Paulo, 2012. Disponível em: <https://www.teses.usp.br/teses/disponiveis/81/81132/tde-25022013-124601/en.php>. Acesso em: 16 nov. 2021. p. 295.
As teorias que sustentam esse modelo teórico, para explicar a influência de certos fatores na velocidade de uma reação química, são as:
(A) Teoria das colisões e Teoria do complexo ativado.
(B) Teoria do estado de transição e Teoria de repulsão dos pares eletrônicos de valência.
(C) Teoria das colisões e Teoria de repulsão dos pares eletrônicos de valência.
(D) Teoria cinética dos gases e Teoria do complexo ativado.
(E) Teoria cinética dos gases e Teoria do estado de transição.
QUESTÃO 3
(UNESP – SP) O esquema apresentado descreve os diagramas energéticos para uma mesma reação química, realizada na ausência e na presença de um agente catalisador.
Com base no esquema, responda qual a curva que representa a reação na presença de catalisador. Explique sua resposta e faça uma previsão sobre a variação da entalpia dessa reação na ausência e na presença do catalisador.
QUESTÃO 4
(UEMG – MG) Considere a seguinte reação reversível genérica:
A + B ⇌ C + D
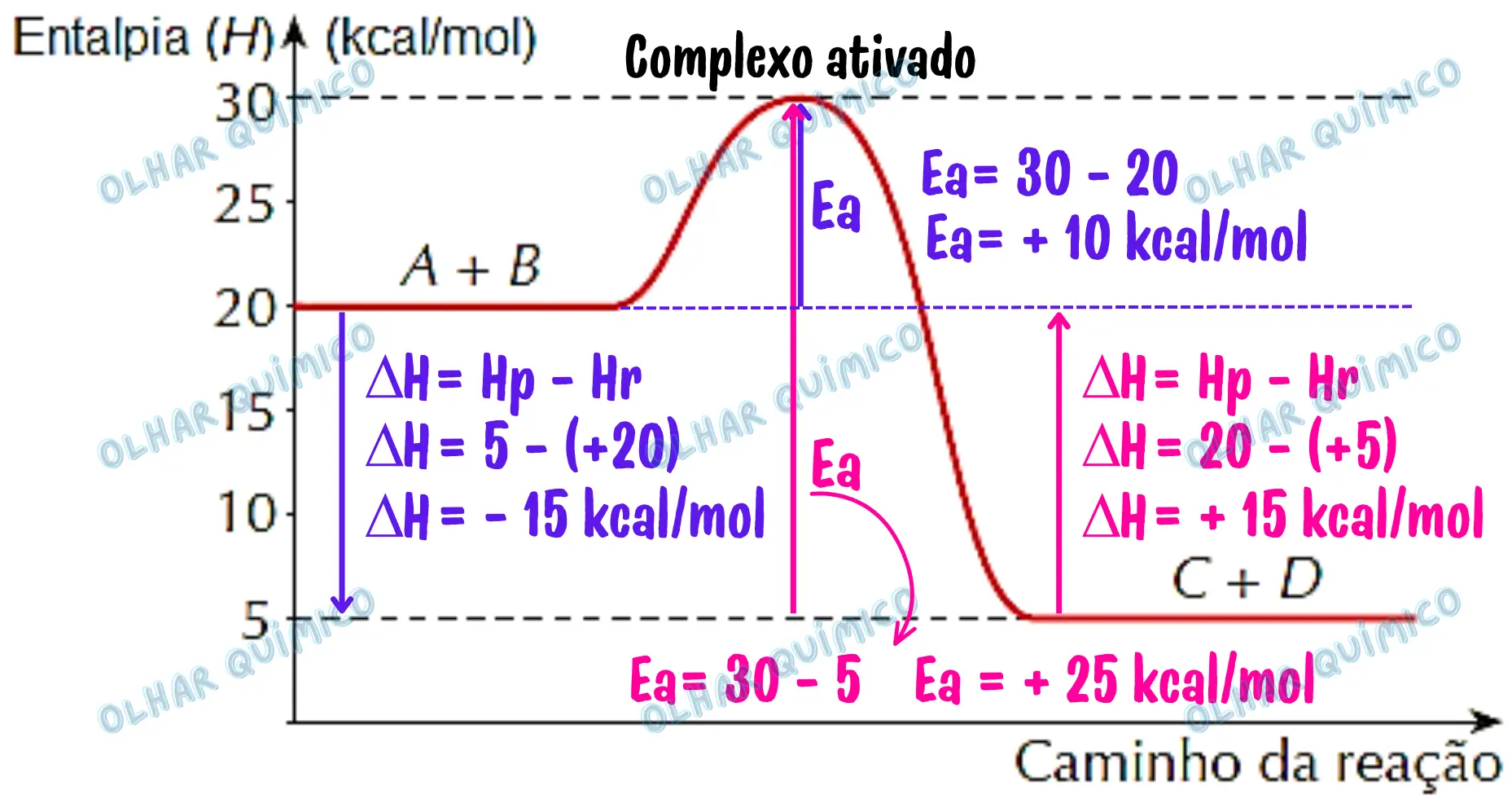
O gráfico termoquímico para essa reação está demonstrado na figura a seguir.
De acordo com os dados do gráfico, assinale a alternativa correta.
(A) A variação de entalpia para a reação direta é igual a + 15 kcal/mol.
(B) A reação inversa libera a mesma quantidade de energia que a reação direta.
(C) A energia de ativação para a reação direta é igual a + 10 kcal/mol.
(D) A variação de entalpia para a reação inversa é igual a + 25 kcal/mol.
QUESTÃO 5
(UFG – GO) A reação química descreve a transformação do composto A em um complexo ativado intermediário que, por sua vez, forma o composto B.
A ⇌ complexo ativado ⇌ B + calor
O gráfico a seguir apresenta a relação entre a energia e o caminho da reação.
Considerando o exposto,
a) calcule a energia de ativação e a variação de entalpia (∆H) da reação.
b) esboce um gráfico entre a energia e o caminho da reação inversa.
QUESTÃO 6
(UPE – PE) A variação de energia para uma dada reação química é apresentada no gráfico ao lado. A partir da leitura desse gráfico, é possível extrair informações quanto à cinética e obter parâmetros termodinâmicos.
Nesse sentido, assinale a alternativa que apresenta a afirmação CORRETA quanto ao processo representado.
(A) O processo ocorre em etapa única e absorve 120 kcal/mol.
(B) O processo ocorre em duas etapas, liberando 250 kcal/mol.
(C) É uma transformação endotérmica que, quando catalisada, tem energia de ativação igual a 110 kcal/mol.
(D) É uma transformação exotérmica que, quando catalisada, tem energia de ativação igual a 120 kcal/mol.
(E) O processo libera 125 kcal/mol, e a reação não catalisada tem energia de ativação igual a 230 kcal/mol.
QUESTÃO 7
(FUVEST – SP) O cientista Richard Feynman, prêmio Nobel de Física em 1965, fez comentários sobre o processo de combustão em uma entrevista chamada Fun to Imagine. Segundo ele, à primeira vista, é impressionante pensar que os átomos de carbono de uma árvore não entram em combustão com o oxigênio da atmosfera de forma espontânea, já que existe uma grande afinidade entre essas espécies para a formação de CO2. Entretanto, quando a reação tem início, o fogo se espalha facilmente.
Essa aparente contradição pode ser explicada pois:
(A) a reação depende de um processo que concentre o carbono para ocorrer.
(B) o fogo torna a reação desfavorável.
(C) o fogo depende da presença de CO2 para começar.
(D) o átomo de carbono da árvore é muito mais resistente ao O2 do que os átomos de carbono dispersos no fogo.
(E) a reação precisa de uma energia de ativação para começar.
QUESTÃO 8
(UEG – GO) Durante a manifestação das reações químicas, ocorrem variações de energia. A quantidade de energia envolvida está associada às características químicas dos reagentes consumidos e dos produtos que serão formados.
O gráfico abaixo representa um diagrama de variação de energia de uma reação química hipotética em que a mistura dos reagentes A e B levam à formação dos produtos C e D.
Com base no diagrama, no sentido direto da reação, conclui-se que a:
(A) energia de ativação da reação sem o catalisador é igual a 15KJ.
(B) energia de ativação da reação com o catalisador é igual a 40KJ.
(C) reação é endotérmica.
(D) variação de entalpia da reação é igual a -30KJ.
QUESTÃO 9
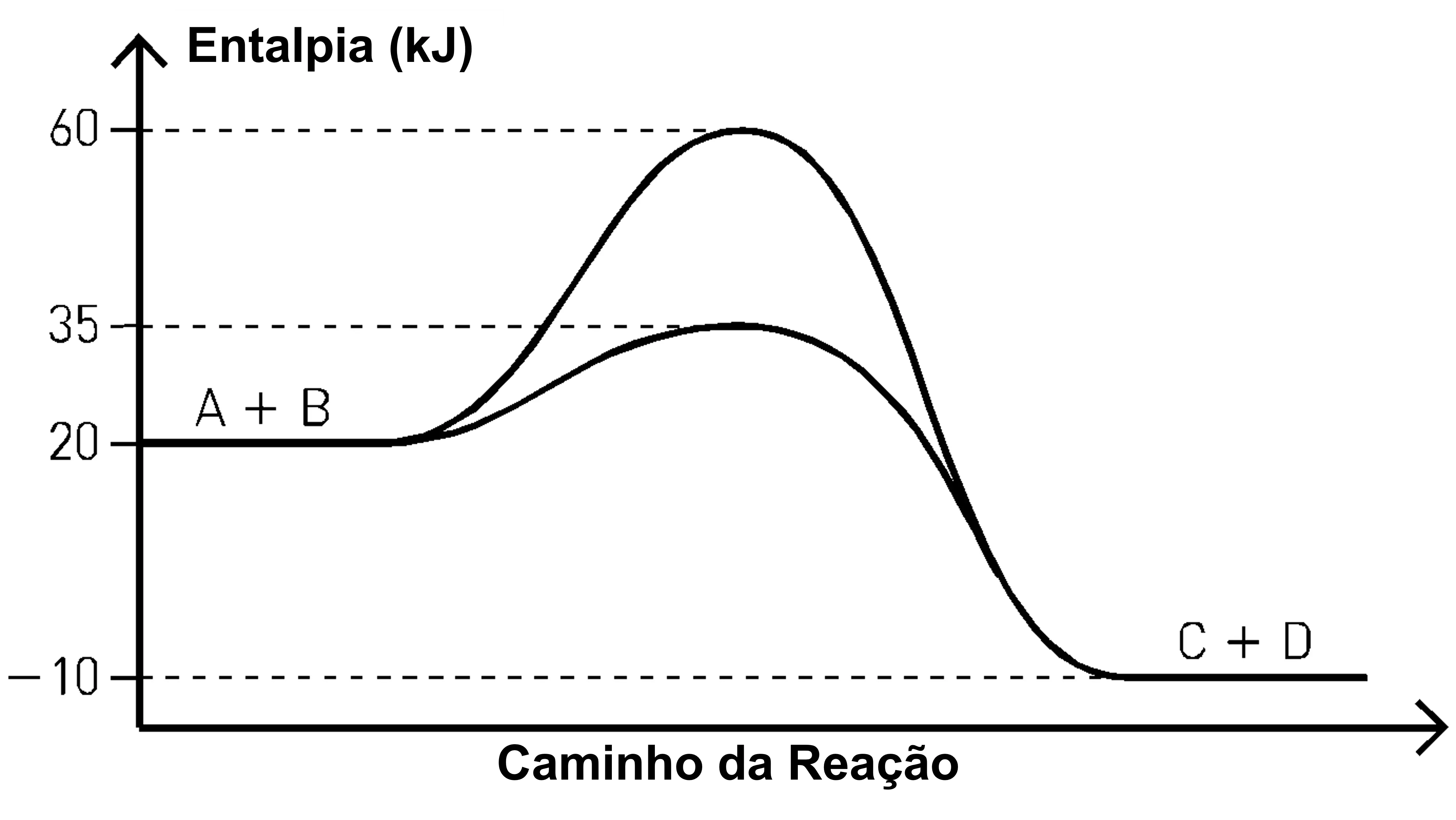
(ENEM) Nos processos de transformação e reciclagem de recursos naturais, as velocidades das reações químicas são estudadas pela cinética química. Uma reação A → B é realizada na presença e na ausência de uma enzima, com todas as demais condições permanecendo inalteradas. Considere que, no gráfico da variação de energia ao longo dessa reação, a linha contínua representa o avanço da reação na ausência da enzima, e a linha pontilhada, na presença da enzima.
O gráfico que representa a situação descrita é:
QUESTÃO 10
(UEL – PR) As figuras X, Y e Z mostram três gráficos de energia em função do progresso da reação. Estas figuras estão representando três reações: R1 → P1; R2 → P2 e R3 → P3.
Com base nas informações contidas nos gráficos, considere as afirmativas a seguir:
I. A energia de ativação da reação R1 → P1 é menor que a energia de ativação da reação R3 → P3.
II. Dentre as reações representadas em X e Z, a reação R3 → P3 é a mais lenta.
III. O valor da energia de ativação das reações representadas nas figuras X, Y e Z depende das concentrações de R1, R2 e R3.
IV. Dentre as três reações, a reação R2 → P2 é a que libera maior quantidade de energia.
Assinale a alternativa correta.
(A) Somente as afirmativas I e II são corretas.
(B) Somente as afirmativas I e III são corretas.
(C) Somente as afirmativas III e IV são corretas.
(D) Somente as afirmativas I, II e IV são corretas.
(E) Somente as afirmativas II, III e IV são corretas.
RESOLUÇÕES E COMENTÁRIOS
QUESTÃO 1
Alternativa D
COMENTÁRIOS
Observe o gráfico para acompanhar a resolução!
(A) Alternativa incorreta. A reação que ocorre pelo caminho II (curva verde) e a que ocorre pelo caminho I (curva vermelha), ambas são exotérmicas.
(B) Alternativa incorreta. O reagente A2 é cosumido mais rapidamente quando a reação ocorre pelo caminho II. Isso ocorre, porque a energia de ativação (Ea) do caminho II, indicada em y, é menor em relação a energia de ativação do caminho I.
(C) Alternativa incorreta. A reação é exotérmica, pois é possível observar no gráfico que a entalpia dos produtos (Hp) é menor do que a entalpia dos reagentes (Hr), em razão da liberação de calor indicada em z, ou seja, o ΔH = – z por mol de A2 consumido.
(D) Alternativa correta. Devido à atuação do catalisador, o caminho II apresenta menor energia de ativação, igual a y, do que o caminho I, cuja energia de ativação é dada por x.
(E) Alternativa incorreta. A reação é exotérmica e libera energia dada por z por mol de A2 consumido. Logo, A2 + B2 → 2 AB ΔH = – z
QUESTÃO 2
Alternativa A
COMENTÁRIOS
A teoria das colisões, prevê que a velocidade da reação depende da influência de alguns fatores, como:
- frequência de colisões (choques eficazes) entre os reagentes;
- energia suficiente (energia de ativação, Ea);
- geometria favorável (orientação adequada).
A presença desses fatores permite a “quebra das ligações químicas” presentes nas moléculas dos reagentes e a formação do complexo ativado (estrutura intermediária entre os reagentes e os produtos).
QUESTÃO 3
COMENTÁRIOS
Observe o gráfico para acompanhar a resolução!
A reação química apresentada no gráfico é realizada na presença e na ausência de um catalisador.
A curva II representa a reação na presença de catalisador. O catalisador é uma substância química capaz de diminuir a energia de ativação (Ea) do sistema e como consequência disso, a reação ocorre mais rapidamente.
Na ausência e presença de catalisador o valor da variação de entalpia da reação permanecerá constante e menor que zero (ΔH < 0), logo a reação é exotérmica. O catalisador não altera a variação de entalpia da reação (ΔH).
COMENTÁRIOS
É importante ter em mente que o catalisador “cria” um caminho alternativo que ocorre com menor energia de ativação (Ea). O catalisador não é consumido durante uma reação química.
QUESTÃO 4
Alternativa C
COMENTÁRIOS
Observe o gráfico para acompanhar a resolução!
Reação direta (violeta) A + B → C + D
Reação inversa (rosa) C + D → A + B
(A) Alternativa incorreta. Na reação direta, A + B → C + D , a variação de entalpia (ΔH) é: ΔH – 15 kcal/mol.
(B) Alternativa incorreta. A reação inversa, C + D → A + B , não libera energia. A reação inversa absorve energia (ΔH = + 15 kcal/mol).
(C) Alternativa correta. A energia de ativação (Ea) para a reação direta é igual a + 10 kcal/mol. Observe os cálculos no gráfico!
(D) Alternativa incorreta. Na reação inversa, a variação de entalpia (ΔH) é: ΔH = + 15 kcal/mol.
QUESTÃO 5
COMENTÁRIOS
Observe o gráfico para acompanhar a resolução!
a)
Cálculo da energia de ativação
Ea = Hcomplexo ativado – Hreagentes
Ea = 60 – 10
Ea = + 50 kJ/mol
Cálculo da variação de entalpia (ΔH)
ΔH = Hp – Hr
ΔH = 30 – (+10)
ΔH = + 20 kJ/mol
b) Gráfico de energia x caminho da reação inversa.
B → A
QUESTÃO 6
Alternativa E
COMENTÁRIOS
O gráfico apresenta uma reação química que foi realizada na presença e ausência de catalisador.
Observe o gráfico para acompanhar a resolução!
(A) Alternativa incorreta. O processo ocorre em uma única etapa, porém com liberação de energia (ΔH = – 125 kcal/mol).
(B) Alternativa incorreta. O processo não ocorre em duas etapas. O processo ocorre em uma única etapa, existindo a reação química catalisada e não catalisada. Ambas com liberação de energia em 125 kcal/mol (ΔH = – 125 kcal/mol).
(C) Alternativa incorreta. A transformação química não é endotérmica. Trata-se de tansformação química exotérmica. Quando catalisada, tem energia de ativação igual a 110 kcal/mol (Ea = + 110 kcal/mol).
(D) Alternativa incorreta. É uma transformação exotérmica que, quando catalisada, tem energia de ativação igual a 110 kcal/mol (Ea = + 110 kcal/mol).
(E) Alternativa correta. O processo libera 125 kcal/mol, e a reação não catalisada tem energia de ativação igual a 230 kcal/mol.
QUESTÃO 7
Alternativa E
COMENTÁRIOS
Mesmo com grande afinidade, os átomos de carbono de uma árvore não entram em combustão com o gás oxigênio da atmosfera, porque não existe a energia de ativação para iniciar a combustão. Para a combustão ocorrer é necessário a energia de ativação. Quando a energia de ativação da reação for alcançada, a reação de combustão terá início, o fogo será espalhado facilmente e o CO₂ será produzido.
QUESTÃO 8
Alternativa D
COMENTÁRIOS
Observe o gráfico para acompanhar a resolução!
A reação química é realizada na presença e na ausência de um catalisador.
(A) Alternativa incorreta. A energia de ativação da reação sem o catalisador é igual a 40 kJ (Ea = + 40 kJ).
(B) Alternativa incorreta. A energia de ativação da reação com o catalisador é igual a 15 kJ (Ea = + 15 kJ).
(C) Alternativa incorreta. A reação é exotérmica. É possível observar no gráfico que a energia dos produtos (– 10 kJ) é menor que a energia dos reagentes (+ 20 kJ), logo ocorreu a liberação de calor (ΔH = – 30 kJ).
(D) Alternativa correta. A variação de entalpia da reação é igual a – 30 KJ (ΔH = – 30 kJ).
QUESTÃO 9
Alternativa C
COMENTÁRIOS
O gráfico da alternativa C é o único que deixa claro o efeito catalítico de uma enzima. Enzimas são catalisadores biológicos. O mecanismo de ação de uma enzima ou catalisador é diminuir a Energia de ativação (Ea) e como consequência, a velocidade da reação química aumenta. As enzimas não alteram a variação de entalpia (ΔH) da reação.
QUESTÃO 10
Alternativa A
COMENTÁRIOS
I. Afirmativa correta. A energia de ativação da reação R1 → P1 (30 kJ/mol) é menor que a energia de ativação da reação R3 → P3 (40 kJ/mol).
II. Afirmativa correta. A energia de ativação da reação R3 → P3, gráfico Z, é de 40 kJ/mol. Já na reação R1 → P1, gráfico X, é de 30 kJ/mol. Portanto, uma reação química com maior energia de ativação ocorre de forma mais lenta!
III. Afirmativa incorreta. A energia de ativação (Ea) não depende das concentrações dos reagentes.
IV. Afirmativa incorreta. A reação R2 → P2 absorve energia (ΔH = + 20 kJ/mol), ou seja, reação endotérmica. A reação R1 → P1 é a que libera maior quantidade de energia (ΔH = – 40 kJ/mol), ou seja, reação exotérmica.
Dúvidas Frequentes sobre Teoria das Colisões
Que tal dar o próximo passo nos seus estudos?
Aprofunde seus conhecimentos e domine este assunto com nossos materiais de apoio.
🎓 EXPLORAR MATERIAIS DE APOIOSua opinião ajuda outros estudantes a encontrarem este conteúdo!
Clique abaixo para deixar seu comentário ou dúvida.
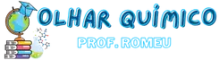




















![Estados Físicos da Matéria: Questões [Provas]](https://olharquimico.com/wp-content/uploads/2020/02/molc3a9culas-de-c3a1gua.jpg)