Na ciência, os estados físicos e mudanças indicam como as partículas de um material se organizam no espaço devido a variações de temperatura e pressão. Essa agitação determina macroscopicamente se o material será sólido (forma e volume definidos), líquido (volume definido, mas forma variável) ou gasoso (forma e volume variáveis).
A grande dificuldade dos estudantes não é decorar os nomes, mas sim entender o comportamento das partículas que sempre aparecem como pegadinhas nas provas de Ciências. Aqui no Olhar Químico, vamos descomplicar esse assunto e preparar você direto para as suas avaliações escolares, traduzindo a teoria de forma simples e visual!
Nesta lista focada nos conceitos essenciais, você vai aprender:
- ✅ Os nomes e as características de cada processo de transição térmica (fusão, solidificação, vaporização, condensação e sublimação).
- 🔥 As transformações térmicas, detalhando o que são processos endotérmicos e exotérmicos.
- 🧊 A diferença estrutural e o grau de agitação das partículas no sólido, líquido e gasoso.
- 📊 A leitura de tabelas com diversas substâncias puras para identificar o estado físico através das temperaturas de fusão e ebulição.
- 🎯 A base teórica completa que irá ajudar você a resolver as questões e converter o que aprendeu em notas excelentes na escola!
👇 Para praticar o conteúdo de hoje: continue rolando a página, resolva os exercícios abaixo e garanta sua nota máxima! 💯📝
🚀 Aviso para alunos do Ensino Médio: se você já domina essa base e quer ir além para testar os seus limites com gráficos e diagramas de fases, recomendo acessar os nossos Exercícios Avançados de Estados Físicos da Matéria para ENEM e Vestibulares.
Resumo Prático: Mudanças de Estado Físico [Para Salvar]

Ter essa tabela salva é o primeiro passo, mas entender como cada transformação ocorre é o que garante a sua nota máxima!
▶️ Dê o play na videoaula completa para nunca mais errar questões sobre os estados da matéria ou…
🎯 Teste os seus conhecimentos com os exercícios práticos logo após o vídeo!
🎬 Videoaula: O Segredo para Não Errar as Mudanças de Estado Físico
Prefere aprender o conteúdo de forma visual e dinâmica antes de testar os seus conhecimentos? Aperte o play na aula exclusiva do canal Olhar Químico.
Neste vídeo, eu vou te mostrar diversos exemplos de mudanças de fase (fusão, vaporização, sublimação, condensação, solidificação) e de transformações endotérmicas e exotérmicas para não cair nas pegadinhas clássicas das provas!
Assistiu à explicação completa e fez as suas anotações? Agora revise a teoria no nosso resumo abaixo e desça a página com a confiança lá em cima para gabaritar a nossa lista de exercícios inéditos! 👇
Você Sabia?
Estados Físicos da Matéria
Existe um estado termodinâmico bizarro chamado Ponto Triplo, onde uma substância consegue ferver e congelar exatamente ao mesmo tempo! Isso ocorre sob condições laboratoriais milimétricas de pressão e temperatura, forçando a matéria a um equilíbrio extremo e fascinante.
No caso da água (a 0,01 °C e 0,006 atm), as três fases — sólido, líquido e gasoso coexistem em perfeita harmonia. Esse fenômeno termodinâmico é tão constante e rigoroso que a ciência o utiliza como o padrão absoluto para calibrar os termômetros de altíssima precisão em todo o mundo!
Resumo: Estados Físicos da Matéria e suas Mudanças
| Estado / Transformação | Definição e Características Principais | Exemplo e Dica para Provas (ENEM) |
|---|---|---|
| Estado Sólido | Possui forma e volume definidos. As partículas estão altamente organizadas em um retículo cristalino com baixíssima energia cinética (apenas vibram). | Cubo de gelo ou barra de metal. Dica: A água é uma exceção anômala; no estado sólido (gelo), é menos densa que no líquido e flutua. |
| Estado Líquido | Possui volume constante, mas forma variável. As partículas deslizam umas sobre as outras, com forças intermoleculares de intensidade intermediária. | Água no copo. Assume o formato do recipiente que a contém devido à fluidez e à ação gravitacional. |
| Estado Gasoso | Possui forma e volume completamente variáveis. As partículas movimentam-se de forma caótica, independente e com altíssima energia cinética. | Vapor d'água ou gás oxigênio. Apresentam alta capacidade de expansão e compressibilidade térmica. |
| Fusão e Solidificação | Fusão é a passagem do sólido para o líquido (processo endotérmico). Solidificação é o retorno do líquido para o sólido (processo exotérmico). | Derretimento de uma vela (Fusão). Formação de gelo no congelador devido à perda de calor (Solidificação). |
| Tipos de Vaporização | Líquido para gás (endotérmico). Divide-se em: Evaporação (lenta, superficial), Ebulição (rápida, com bolhas) e Calefação (choque térmico instantâneo). | Roupa secando no varal (evaporação) x Água fervendo a 100 °C (ebulição) x Gota d'água caindo em chapa superaquecida (calefação). |
| Sublimação e Condensação | Sublimação é a passagem direta do sólido ao gás (sem passar pelo líquido). Condensação (ou Liquefação) é a passagem do gás ao líquido (exotérmico). | Pastilhas de naftalina "sumindo" nas gavetas (Sublimação). Gotículas de "suor" na parte externa do copo de refrigerante gelado (Condensação). |
| Curva de Aquecimento | Gráfico que relaciona a temperatura com a quantidade de calor. Durante as mudanças de fase de uma substância pura, o patamar horizontal se mantém fixo. | Pegadinha do ENEM: Se houver variação de temperatura durante a fusão ou ebulição, o sistema analisado é uma mistura, não uma substância pura. |
Chegou a hora de testar os seus conhecimentos na prática!
Nesta lista de exercícios, ao responder cada questão, você terá acesso imediato ao gabarito e ao Comentário do Professor Romeu com a resolução passo a passo para você entender o conteúdo e não cair nas clássicas pegadinhas de ENEM, vestibulares e provas escolares!
Pronto para gabaritar as 15 questões de Química?
Leia o enunciado, escolha a sua alternativa e inicie o seu teste abaixo!
15 Exercícios sobre Fusão, Evaporação, Condensação, Sublimação e Solidificação com Gabarito Comentado
 Dentre esses processos, os que envolvem, respectivamente, absorção e liberação de calor são:
Dentre esses processos, os que envolvem, respectivamente, absorção e liberação de calor são:Mas por que as outras alternativas estão incorretas? Vamos analisar os erros! Compare as afirmações corrigidas abaixo com as opções da questão:
(B) Corrigida. A mudança do estado sólido para o estado líquido chama-se fusão.
(C) Corrigida. A densidade da água no estado sólido é MENOR que no estado líquido.
(D) Corrigida. A passagem do estado líquido para o estado gasoso chama-se vaporização e que pode ser: evaporação, ebulição e calefação.
(E) Corrigida. A água ganha calor (endotérmico) no processo de mudança do estado sólido para o estado líquido.
No estado líquido, as partículas encontram-se um pouco mais afastadas e desorganizadas, permitindo que a matéria tenha volume definido, mas assuma a forma do recipiente que ocupa. Já no estado gasoso, as partículas estão muito afastadas e movimentam-se livremente, resultando em um estado sem forma nem volume definidos, ocupando o espaço disponível.
Observe o diagrama a seguir:
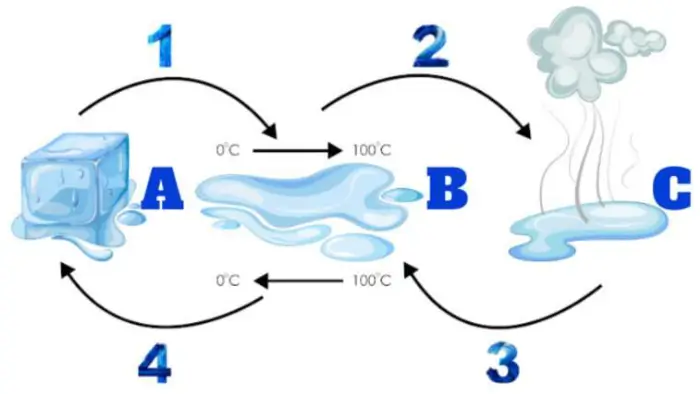
Quais as mudanças de estado físico da matéria são representadas respectivamente pelos números 1 e 4?
Mudança 1 – água formada na superfície externa de um copo.
Mudança 2 – água proveniente do derretimento de gelo.
 De acordo com as informações fornecidas, afirma-se que nas mudanças citadas ocorre:
De acordo com as informações fornecidas, afirma-se que nas mudanças citadas ocorre: Pela análise dos dados da tabela, medidos a 1 atm, podemos afirmar que à temperatura de 40 °C e 1 atm:
Pela análise dos dados da tabela, medidos a 1 atm, podemos afirmar que à temperatura de 40 °C e 1 atm: Veja a resolução apresentada na tabela acima e em caso de dúvidas para resolver esse tipo de questão, siga esses 3 passos simples para não cair em pegadinhas:
Veja a resolução apresentada na tabela acima e em caso de dúvidas para resolver esse tipo de questão, siga esses 3 passos simples para não cair em pegadinhas:1. Análise do Dado: temperatura fornecida de 40 °C
2. Comparação: compare a temperatura fornecida com o Ponto de Fusão (PF) e o Ponto de Ebulição (PE) da tabela.
3. Conclusão: nessa questão:
álcool: 40 °C está ENTRE –117 °C (ponto de fusão) e 78 °C (ponto de ebulição), portanto o álcool se encontra na fase líquida.
éter etílico: 40 °C está ACIMA de –34 °C (ponto de ebulição), logo o éter etílico se encontra na fase gasosa.
Considere os dados das três substâncias seguintes:
 É correto afirmar que em um ambiente a 35 °C, sob pressão atmosférica, as substâncias I, II e III apresentam-se, respectivamente, nos estados físicos:
É correto afirmar que em um ambiente a 35 °C, sob pressão atmosférica, as substâncias I, II e III apresentam-se, respectivamente, nos estados físicos:
Observe a resolução na tabela acima e siga esses 3 passos simples para não cair em pegadinhas:
1. Análise do Dado: temperatura fornecida de 35 °C
2. Comparação: compare a temperatura fornecida com o Ponto de Fusão (PF) e o Ponto de Ebulição (PE) da tabela.
3. Conclusão: nessa questão:
estanho: 35 °C está ABAIXO de 232 °C (ponto de fusão), portanto o estanho será sólido.
flúor: 35 °C está ACIMA de – 188 °C (ponto de ebulição), então o flúor estará no estado gasoso.
césio: 35 °C está ENTRE os valores de 28 °C (ponto de fusão) e 678 °C (ponto de ebulição), assim o césio estará no estado líquido.
( ) Uma substância que se encontra inicialmente na fase vapor libera calor ao condensar.
( ) Um líquido incolor é submetido a um aquecimento suave até que entra em ebulição, quando então sua temperatura continua a aumentar gradualmente. Trata-se, portanto, de uma solução.
( ) A evaporação, uma passagem do estado líquido para o vapor, somente ocorre, para a água, acima de 100 °C, assim como a ebulição.
( ) A constância da temperatura de fusão de um sólido é um dos critérios usados para estabelecer a pureza dessa substância.
A sequência correta de preenchimento dos parênteses, de cima para baixo, é:
(V): A condensação é uma transformação exotérmica (libera calor).
(V): As substâncias puras possuem temperatura de ebulição fixa durante o aquecimento. Como a temperatura aumentou gradualmente durante a ebulição, trata-se de misturas homogêneas ou soluções.
(F) Corrigida: A evaporação ocorre em qualquer temperatura de maneira lenta e sem a formação de bolhas. A ebulição da água é 100 °C a 1 atm, caso a pressão seja reduzida, a água entrará em ebulição abaixo de 100 °C.
(V): As substâncias puras possuem temperatura de fusão e ebulição fixas (constantes) e essa propriedade é fundamental para estabelecer a pureza de uma substância qualquer.
 De acordo com a tabela, a 35,5 °C, encontram-se no estado líquido apenas as substâncias:
De acordo com a tabela, a 35,5 °C, encontram-se no estado líquido apenas as substâncias:
Observe a resolução na imagem da tabela acima e siga esses 3 passos simples que considero muito importante para não cair em pegadinhas até mesma do ENEM:
1. Análise do Dado: temperatura fornecida de 35,5 °C
2. Comparação: sempre compare a temperatura fornecida com o Ponto de Fusão (PF) e o Ponto de Ebulição (PE) da tabela.
3. Conclusão: nessa questão:
bromo: 35,5 °C está ENTRE –7,2 °C (ponto de fusão) e 58,8 °C (ponto de ebulição), logo o bromo se encontra no estado líquido.
metanol: 35,5 °C está ENTRE –97 °C (ponto de fusão) e 64,7 °C (ponto de ebulição), portanto o metanol se encontra no estado líquido.
amônia: 35,5 °C está ACIMA de –33,4 °C (ponto de ebulição), assim a amônia se encontra no estado gasoso.
flúor: 35,5 °C está ACIMA de –188,1 °C (ponto de ebulição), logo o flúor se encontra no estado gasoso.
oxigênio: 35,5 °C está ACIMA de – 183,0 °C (ponto de ebulição), portanto o flúor se encontra no estado gasoso.
Vamos analisar os erros em cada alternativa! Compare as afirmações corrigidas abaixo com as opções da questão:
(B) Corrigida: A passagem de gotículas de água (líquido) para cristais de gelo (sólido) é o processo de solidificação.
(C) Corrigida: Gotículas minúsculas se unindo para formar gotas pesadas de chuva não é uma mudança de estado físico, mas sim um fenômeno mecânico de coalescência (ou aglutinação).
(D) e (E) Corrigida: O resfriamento do vapor de água (estado gasoso) em baixas altitudes para formar neblina ou orvalho (estado líquido), ilustra perfeitamente a condensação.
- 1º Fenômeno (Roupas no varal): A água líquida presente nas roupas absorve o calor do ambiente (processo endotérmico) e passa para o estado gasoso de forma lenta e espontânea, abaixo da temperatura de fervura. Esse processo natural é a evaporação.
- 2º Fenômeno (Tampa da panela): O vapor de água que sobe do arroz encontra a superfície da tampa que está ligeiramente mais fria (menos calor). Ao perder calor (processo exotérmico), o vapor retorna ao estado líquido, formando as gotas de água. Esse fenômeno é a condensação.
Sua Nota Final
📚 Continue Estudando: Aprenda também estes assuntos!
Dominar os estados físicos da matéria vai muito além de decorar nomes como fusão ou sublimação. 🧠 É entender como a energia térmica e a pressão transformam os fenômenos físicos ao nosso redor! 🌍
Como na natureza as substâncias puras raramente estão sozinhas, o seu próximo passo é entender o que acontece quando unimos diferentes materiais (como no estudo das Misturas e Métodos de Separação). 🧪
Preparado para subir o nível? 🚀
Escolha seu próximo destino abaixo e continue sua jornada de estudos no Olhar Químico: 👇
Dúvidas Frequentes sobre Estados Físicos da Matéria
A principal diferença está na energia cinética das partículas e na força de atração entre elas. No estado sólido, as partículas apenas vibram em posições fixas. No líquido, elas possuem maior liberdade e deslizam umas sobre as outras. Já no estado gasoso, a atração é quase nula e o movimento é rápido e caótico.
Em uma curva de aquecimento de substância pura, as mudanças de estado físico (como fusão e ebulição) ocorrem com temperatura constante. Isso forma patamares horizontais no gráfico, pois todo o calor recebido, chamado de calor latente, é usado exclusivamente para romper as interações intermoleculares, e não para aumentar a temperatura.
As três são formas de vaporização. A evaporação é lenta e ocorre apenas na superfície do líquido. A ebulição é rápida, turbulenta e ocorre em toda a massa líquida (formando bolhas) ao atingir uma temperatura específica. A calefação é instantânea, acontecendo por choque térmico quando o líquido toca uma superfície muito mais quente que seu ponto de ebulição.
Isso ocorre devido ao comportamento anômalo da água. Ao congelar, as pontes de hidrogênio organizam as moléculas em uma estrutura cristalina hexagonal com muitos espaços vazios. Isso faz com que o gelo tenha um volume maior e, consequentemente, uma densidade menor do que a água líquida, permitindo que ele flutue.
A sublimação é a passagem direta de uma substância do estado sólido para o estado gasoso, sem passar pela fase líquida. É um processo endotérmico (absorve calor). O exemplo mais clássico cobrado no ENEM são as bolinhas de naftalina deixadas em gavetas, que diminuem de tamanho à medida que liberam vapor, ou o gelo seco.
Que tal dar o próximo passo nos seus estudos?
Aprofunde seus conhecimentos e domine este assunto com nossos materiais de apoio.
🎓 EXPLORAR MATERIAIS DE APOIOSua opinião ajuda outros estudantes a encontrarem este conteúdo!
Clique abaixo para deixar seu comentário ou dúvida.



![Estados Físicos da Matéria: Questões [Provas]](https://olharquimico.com/wp-content/uploads/2020/02/molc3a9culas-de-c3a1gua.jpg)